关于举办“体外诊断试剂研发与法规公益培训班”通知 日期:2023-03-30 浏览:714
各有关单位:
体外诊断产品作为医疗器械领域发展速度最快、势头最好的细分行业,倍受医院、投资者和企业的关注,新冠肺炎疫情爆发使得体外诊断试剂行业进入大众视野。为指导体外诊断试剂注册工作,国家药品监督管理局于2021年发布了《体外诊断试剂注册与备案管理办法》《体外诊断试剂临床试验技术指导原则》《免于临床试验的体外诊断试剂临床评价技术指导原则》等部门规章及指导原则,新法规频发、监管态势加剧从严,体外诊断试剂企业在产品注册过程中出现了性能研究不合规、临床评价指标选择错误、原材料管理不当等诸多共性问题。
为帮助体外诊断试剂生产企业完善对体外诊断试剂的设计与开发流程学习,了解体外诊断试剂注册的基础法规,提高注册申报工作的质量和效率,中国食品药品企业质量安全促进会医疗器械分会联合北京亦庄生物医药园定于2023年4月19日在北京举办“体外诊断试剂研发与法规公益培训班”。
具体内容如下:
一、组织架构
主办单位:
中国食品药品企业质量安全促进会医疗器械分会
北京亦庄生物医药园
学术支持:
北京市药监局医疗器械审评核查中心
武汉致众科技股份有限公司
北京嘉华汇诚科技股份有限公司
微珂医药技术服务(上海)有限公司
二、日程安排
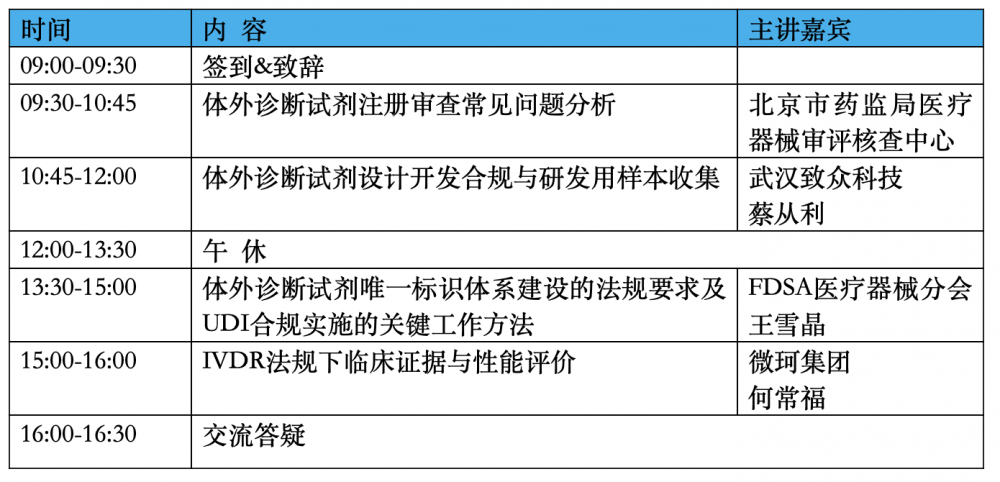
三、培训对象
体外诊断试剂及仪器生产研制单位法规人员、注册人员、研发人员、质量体系等相关人员。
四、时间地点
时间:2023年4月19日(全天)
地点:北京亦庄生物医药园(北京经济技术开发区科创六街88号)
五、报名方式

本次培训为公益活动、微信扫码报名
六、联系方式:
联系人:孙亚宾
座 机:010-52134332 13552226832(同微信)
邮 箱:yiliaoqixiefenhui@126.com
中国食品药品企业质量安全促进会医疗器械分会
2023年3月28日
上一篇:关于准予成立细胞医药分会的批复