关于举办第二届“有源医疗器械注册检验及电气安全技术论坛”通知 日期:2022-12-07 浏览:952
各有关单位:
原定于在86届CMEF展会期间举办的第二届“有源医疗器械注册检验及电气安全技术论坛”,因疫情原因改为线上,日程安排不变。
具体通知如下:
一、组织架构
主办单位:
中国食品药品企业质量安全促进会医疗器械分会
国药励展有限责任公司
学术支持:
中国食品药品检定研究院
迈迪思创(北京)科技发展有限公司
苏州熠品质量技术服务有限公司
英格尔集团·敏业信息
DEKRA德凯
二、时间及授课方式
时 间:2022年12月23日(全天)
授课软件:腾讯会议
三、论坛日程
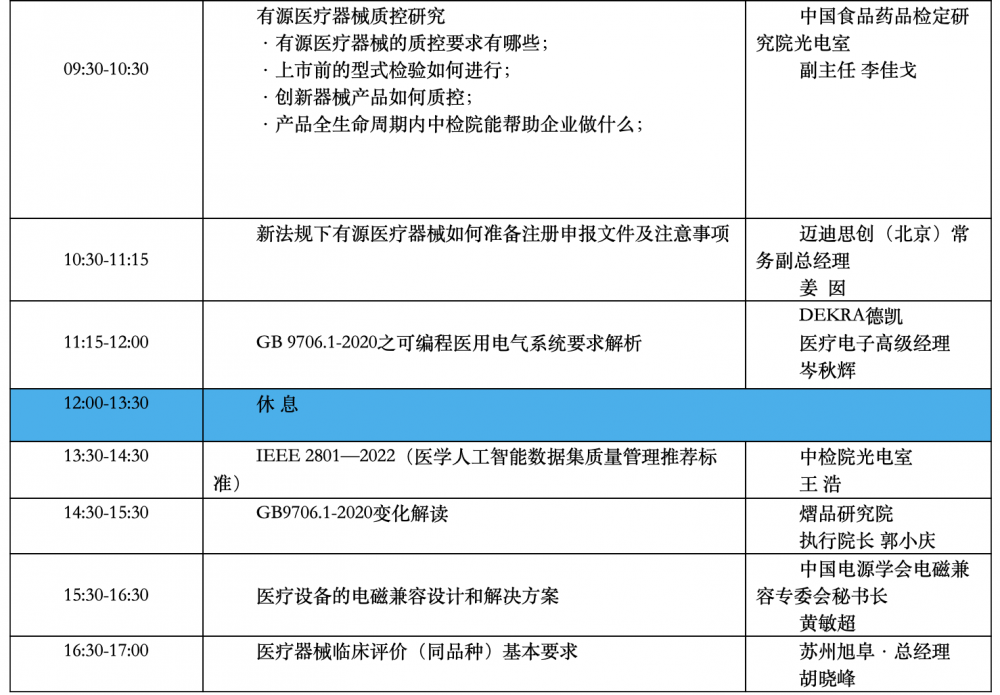
四、讲师介绍
李佳戈
中国食品药品检定研究院,光电室副主任;生物医学工程专业硕士,高级工程师;全国医用电器标准化技术委员会(SAC/TC10)委员;全国医用电器标准化技术委员会医用电子仪器标准化分技术委员会(SAC/TC10/SC5)委员;中国医学装备学会应急救治装备分会常委;《中国医药导刊》编委;
2004年进入中国食品药品检定研究院工作,先后从事过无源医疗器械检验、医疗器械产品行政审批及有源医疗器械检验工作。主持国家级课题1项、省部级课题1项;参加国家“863”项目1项、科技支撑项目2项。在国家级刊物上以第一作者或通讯作者发表文章20余篇,作为执行主编、副主编及编委出版书籍4册。。目前主要从事有源医疗器械性能、安全和电磁兼容的检测及质量控制工作。
姜 囡
迈迪思创(北京)科技发展有限公司常务副总经理;14年医疗器械产品注册经验,精通I/II/III类器械备案和注册流程,负责及参与管理注册项目700多个,产品类型包括有源、无源、三类植入类医疗器械。注册申报形式涵盖NMPA所有申报形式。曾参与多项医疗器械产品的审评指导原则和医疗器械国家、行业标准的起草、修订和技术讨论工作会议。
岑秋辉
DEKRA德凯广州医疗电子高级经理;从事医疗器械检测和认证工作14年,具有丰富的医疗器械安规和性能的检测经验以及解决方案设计。为近百家国内外企业服务,并获得客户的好评。
王 浩
中国食品药品检定研究院副研究员;美国波士顿大学博士,美国哈佛医学院博士后;全国人工智能医疗器械标准化技术归口单位秘书长;IEEE人工智能医疗器械标准工作组组长;IEC TC62委员会软件网络与人工智能顾问组专家;
主要从事人工智能医疗器械标准化与质量研究工作;主持国家重点研发计划课题一项和多项省部级课题,在国内外学术期刊和会议发表论文30余篇,拥有PCT国际发明专利1项。主持制订四项人工智能医疗器械行业标准、两项IEEE 人工智能医疗器械国际标准。
郭小庆
生物医学工程硕士;现任熠品集团技术副总;熠品研究院执行院长;全国标准化委员会TC27/SC4委员;长期从事医疗器械安全和有效性评价。
黄敏超
中国电源学会电磁兼容专委会秘书长;IEEE会员和南京航空航天大学研究生企业课程讲师和上海海事大学外聘硕士生导师;1998年浙江大学博士,现担任敏业信息科技的首席咨询师,具有丰富的电磁兼容的理论与实践经验,拥有多项国内外专利及软件版权,在国内外学术期刊和国际会议上发表多篇论文。
胡晓峰
苏州大学MBA;德能医学服务集团副总经理/合伙人;苏州旭阜医疗器械技术服务有限公司 总经理;10余年医疗器械项目管理经验,对医疗器械全生命周期的运营有着丰富的经验,擅长策划医疗器械产品上市的整体解决方案。
五、报名方式

本次论坛免费、微信扫码报名、论坛前一天短信发送链接。
六、联系方式
联系人:孙老师
电 话:13552226832(同微信)
邮 箱:yiliaoqixiefenhui@126.com
![]() 关于举办第二届“有源医疗器械注册检验及电气安全技术论坛通知”.pdf
关于举办第二届“有源医疗器械注册检验及电气安全技术论坛通知”.pdf
中国食品药品企业质量安全促进会医疗器械分会
2022年12月6日