第30期“医疗器械唯一标识(UDI)实施与合规公益培训班”通知 日期:2023-03-30 浏览:529
各有关单位:
2021年1月1日,第一批9大类69个品种开始实施医疗器械唯一标识。2022年6月1日,其他第Ⅲ类医疗器械(含体外诊断试剂)作为第二批实施品种全面实施医疗器械唯一标识,2024年6月1日第三批实施目录包含Ⅱ类141个产品,在产品上市销售前,注册人应当按照相关标准或者规范要求将最小销售单元、更高级别包装的产品标识和相关数据上传至医疗器械唯一标识数据库,确保数据真实、准确、完整、可追溯。为帮助企业(Ⅱ类产品)解决UDI实施过程中的问题,中国食品药品企业质量安全促进会医疗器械分会联合广东省医疗器械行业协会定于2023年4月4日在广州举办第30期“医疗器械唯一标识(UDI)实施与合规公益培训班”,培训班围绕GS1标准、国家局数据库操作、标签模板、标签检测、防串货、如何选择打印设备等实施问题进行讲解。会议信息如下:
一、组织架构
主办单位:
中国食品药品企业质量安全促进会医疗器械分会
广东省医疗器械行业协会
学术支持:
长沙睿展数据科技有限公司(GS1供应商)
上海沁晶自动化科技有限公司
广州慧翼智能科技有限公司
二、培训内容
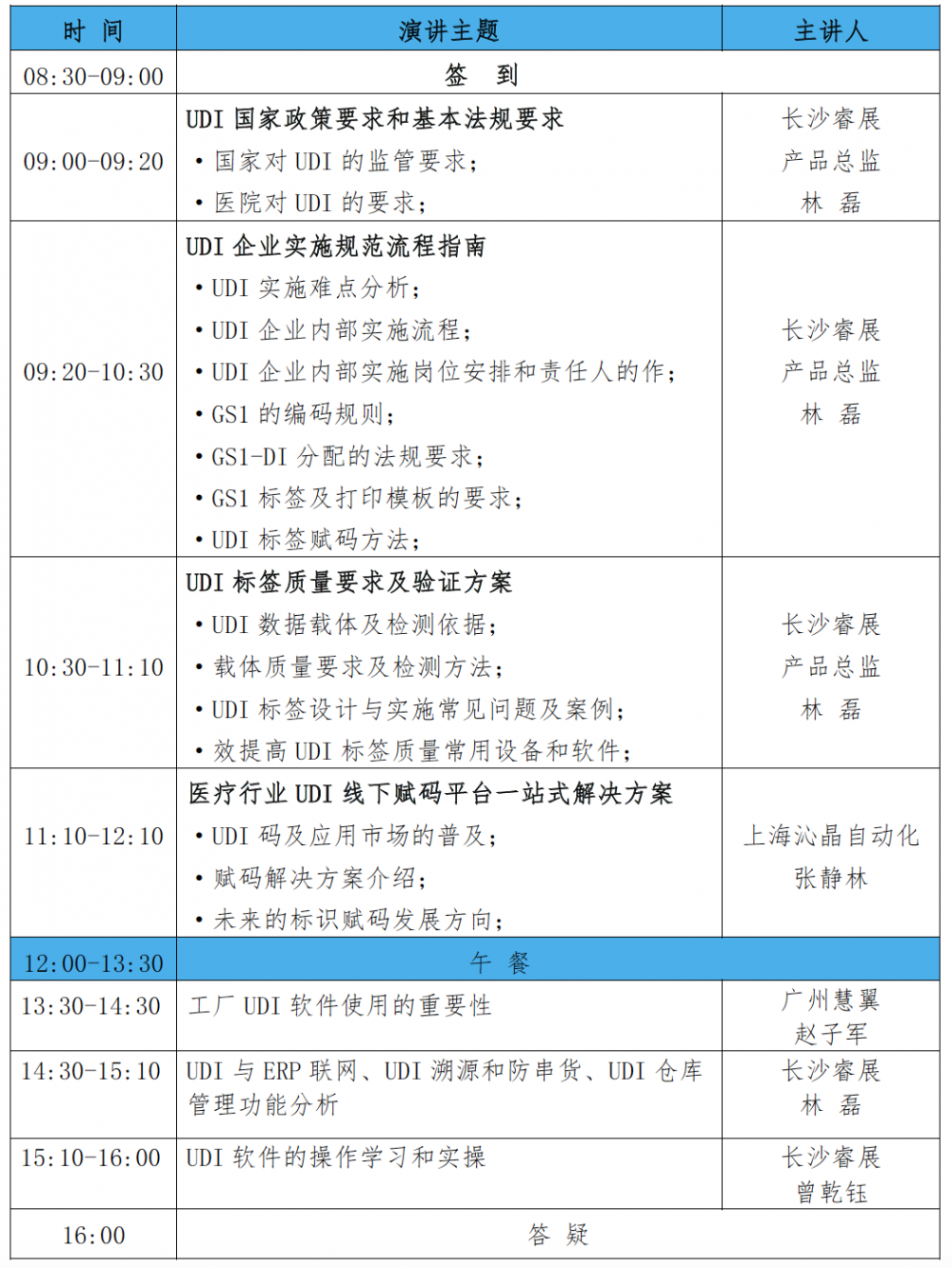
三、培训对象
从事医疗器械注册、研发、管理、质量法规、临床、及生产相关人员;生产或经营药品、疫苗及医疗器械产品的企业相关人员;
四、培训意义
1、掌握医疗器械UDI相关法律法规知识
2、简化申报流程,节约申报时间成本和人工成本,提高申报效率
3、提升企业信息化水平,提高企业生产效率
五、时间地点
时 间:2023年4月4日
地 点:具体地点以电话或短信通知
六、报名方式

本次培训为公益活动、不收取任何费用
微信扫码报名
七、联系方式
中国食品药品企业质量安全促进会医疗器械分会
联系人:孙亚宾
电 话:010-52134332 13552226832(同微信)
邮 箱:yiliaoqixiefenhui@126.com
广东省医疗器械行业协会
联系人:马海薇
电 话:020-87006574 13632328457(同微信)
邮 箱:2651247614@qq.com
中国食品药品企业质量安全促进会医疗器械分会
广东省医疗器械行业协会
2023年3月17日