第二届“全球医疗器械法规论坛” 通知 日期:2023-04-20 浏览:596
各有关单位:
自2020年新冠疫情全球爆发以来、医疗器械出口持续增加,国产医疗器械迎来前所未有的发展机遇,多国家法规不同对企业产品认证带来很大挑战。为帮助中国医疗器械企业了解国际医疗器械法规,中国食品药品企业质量安全促进会医疗器械分会联合国药励展定于87届CMEF展会期间举办第二届“全球医疗器械法规论坛”,论坛将围绕欧盟MDR、巴西IVDR、美国FDA、加拿大等方面进行分享。
具体内容如下:
一、组织架构
主办单位:
中国食药促进会医疗器械分会
国药励展展览有限责任公司
学术支持:
英格尔集团
德国莱茵TÜV有限公司
上海沙格医疗科技有限公司
羚证医药技术服务(上海)有限公司
深圳市卓远天成咨询有限公司
深圳市瑞恩尼医疗器械管理咨询有限公司
二、时间地点
时 间:2023年5月14日(全天)
地 点:上海国家会展中心·M203会议室(会展大道1-2号馆层)
三、培训内容
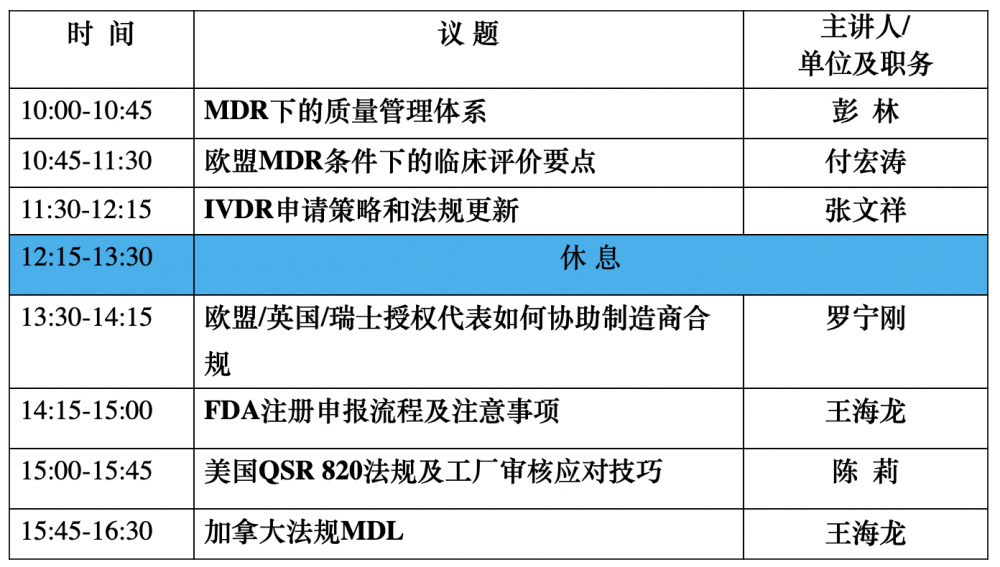
四、嘉宾介绍
彭 林
羚证医药技术服务(上海)有限公司技术经理;微生物学硕士、多年的灭菌站工作经验;200+企业辅导经验;13年医疗器械从业经验,熟练掌握医疗器械法规,多年CE认证和ISO13485认证经验。熟练掌握ISO13485/MDSAP医疗质量管理体系;精通无菌医疗器械微生物和灭菌等要求;熟练掌握特殊过程和关键工序的验证及设备确认等要求。擅长:欧盟医疗器械法规、ISO13485质量管理体系、ISO14971风险管理、临床评价及上市后监督、无菌医疗器械相关测试和验证等。
付宏涛
深圳市卓远天成咨询有限公司总咨询师;1998年进入医疗器械行业,国内从事FDA 510(k)、QSR820、医疗器械CE认证的先行者之一。精通美国、欧盟、巴西、中国、日本、加拿大、澳大利亚等多国医疗器械(含IVD)法规及通用标准,十多年来,亲手完成CE认证、FDA 510(k)、QSR820验厂辅导等各类案例百余起,无一失败。先后被TUV Rheinland、BSI、SGS等国际机构聘为医疗器械法规讲师或专家小组成员,是医疗器械国际法规咨询行业为数不多的实战派专家之一。
张文祥
德国莱茵TÜV有限公司 MD/IVD产品颁证官;德国莱茵TÜV北方区经理(医疗),大中华区体外诊断产品协调人;十年以上公告机构从业经验,疫情期间支持推动国内优秀企业进行疫情产品欧盟CE认证。
罗宁刚
SUNGO公司联合创始人,国内知名高校硕士研究生;IEC认证机构国际评审员,获IEC颁发的IEC 1906奖章;曾长期任职于知名认证机构亚太总部,分管全球产品认证和亚太区分支机构业务;在长期与海外医疗监管当局协作中积累了丰富的医疗器械国际注册经验,能够为企业产品出海提供最佳的注册方案。
陈 莉
英格尔集团法规总监,美国Northeastern University医疗法规专业理学硕士,从事医疗器械法规服务6年,推动上市的产品涉及:动物源,植入类,体外诊断,普外科品药械组合等方面。熟悉美国,欧盟,韩国,日本,马来西亚,印尼等国家法规要求,多次成功助力企业顺利通过FDA现场飞行检查。
王海龙
瑞恩尼咨询创始人/总经理/总顾问;多家公告机构特聘讲师;2005年从事医疗器械法规工作至今,具有深厚的医疗器械注册、法规、体系与质量管理经验;具有多年医疗器械企业高层管理经验,熟悉医疗器械公司各部门的运转流程与业务要求;独立完成NMPA,CE,FDA 510K,MDSAP以及FDA工厂检查等百余例项目,至今保持着辅导与注册零失败案例;医疗器械行业的实战专家,从理论到实践知行合一。
五、报名方式

本次论坛免费、大家扫码报名。
六、联系方式
联系人:张老师
电 话:010-52134332
邮 箱:yiliaoqixiefenhui@126.com
中国食药促进会医疗器械分会
2023年4月20日