第四届“医疗器械唯一标识(UDI) 实施与合规论坛”通知 日期:2023-04-20 浏览:750
各有关单位:
2021年1月1日,第一批9大类69个品种开始实施医疗器械唯一标识。2022年6月1日,其他第Ⅲ类医疗器械(含体外诊断试剂)作为第二批实施品种全面实施医疗器械唯一标识,2024年6月1日第三批实施目录包含Ⅱ类141个产品,在产品上市销售前,注册人应当按照相关标准或者规范要求将最小销售单元、更高级别包装的产品标识和相关数据上传至医疗器械唯一标识数据库,确保数据真实、准确、完整、可追溯。为帮助Ⅱ类企业解决UDI实施的问题,中国食品药品企业质量安全促进会医疗器械分会联合国药励展定于87届CMEF展会期间举办第四届“医疗器械唯一标识(UDI)实施与合规论坛”,坛将围绕UDI设计,从基本概念到应用实施,针对UDI编码、UDI标签设计、上报数据库、UDI扩展应用、产品溯源防伪等全方位分享。
具体通知如下:
一、组织架构
主办单位:
中国食药促进会医疗器械分会
国药励展展览有限责任公司
学术支持:
北京爱创科技股份有限公司
北京嘉华汇诚科技股份有限公司
湖南中广汇智信息技术有限公司
南通慧羽智能科技有限公司
二、时间地点
时 间:2023年5月14日(全天)
地 点:上海国家会展中心·M103会议室(会展大道1-2号馆层)
三、论坛日程
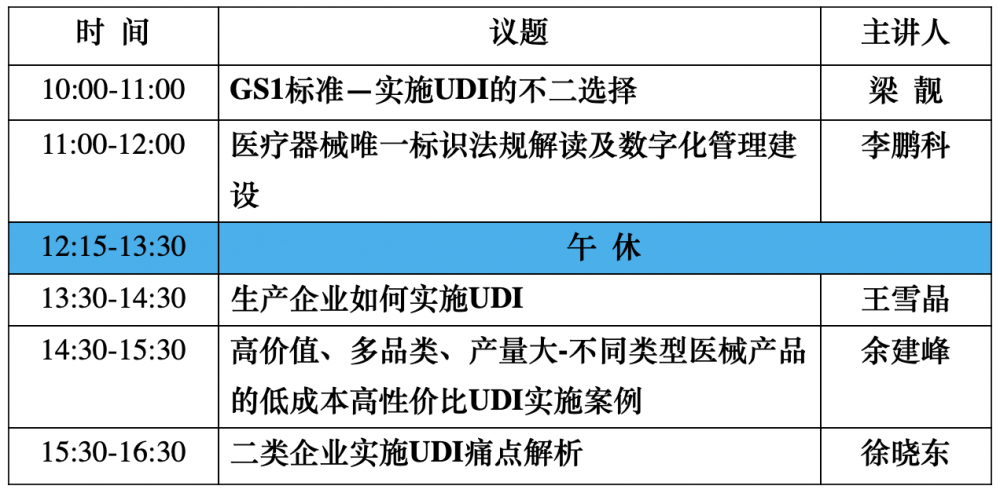
四、嘉宾介绍
梁 靓
中国物品编码中心(上海分中心)UDI专员;从事GS1标准体系在零售、医疗、物流业推广及培训工作已有17年。自2007年参与GS1系统在植入性医疗器械监管的应用项目以来,积累了丰富的医疗器械编码追溯的应用及培训经验。2016年被评为中国物品编码中心高级培训教师,主要负责上海地区的UDI工作,帮助企业正确实施UDI。
李鹏科
北京爱创科技股份有限公司解决方案专家;医疗器械及快消品领域追溯体系建设专家,曾主导实施多家生产及追溯系统,十多年自动识别领域售前及实施经验,为众多行业龙头企业提供咨询及技术解决方案。
王雪晶
中国食品药品企业质量安全促进会医疗器械分会副秘书长;北京嘉华汇诚联合创始人之一,在医药追溯领域从业17年;熟悉中国、美国、欧盟医药器械供应链安全追溯法规及系统建设,带领团队已为制药行业超50%企业提供合规咨询及追溯系统建设服务、获得中国唯一欧盟EU-HUB接入授权、美国GS1 DSCSA认证。熟悉医疗器械UDI法规及UDI实施的关键方法,自2019年医疗器械UDI试点至今,带领团队深度研究、不断探索和实践,已帮助覆盖行业全链条的众多国内国际企业成功实施UDI。
余建峰
中广汇智UDI公共平台资深讲师;专注企业数字化升级、生产线改造落地实施;累计组织UDI公益培训60+场,培训企业超过6000家;累计服务企业UDI合规赋码及生产线改造超过200家;
徐晓东
南通慧羽智能科技有限公司创始人;高级工程师、工业可变数据打印行业14年从业经验;参与了药品电子监管码等行业溯源的落地实施工作;医疗器械UDI实施近百家企业实施经验。
五、报名方式

本次论坛免费、大家扫码报名。
六、联系方式
联系人:张老师
电 话:010-52134332
邮 箱:yiliaoqixiefenhui@126.com
![]() CMEF“医疗器械唯一标识(UDI)实施与合规论坛”.pdf
CMEF“医疗器械唯一标识(UDI)实施与合规论坛”.pdf
中国食药促进会医疗器械分会
2023年4月20日