“卓识远见,传承创新”系列公益讲座第十五期中医循证与临研质控专场顺利举办 日期:2023-06-21 浏览:804
2023年06月20日,由中国食品药品企业质量安全促进会、中国医药新闻信息协会指导,中国食药促进会临床研究管理专业委员会主办、北京卓越未来国际医药科技发展有限公司承办、北京亦庄国际投资发展有限公司协办的“卓识远见,传承创新”系列公益讲座第十五期在云端与各位同行如约而至。本期讲座特邀天津中医药大学中医药研究院院长张俊华教授、广西医科大学第一附属医院国家药物临床试验机构办公室周燕文主任分别就《中医药循证评价的关键问题》、《临床试验的“源”》进行授课。现进行学术专场要点回顾。本场专题讲座主持人为北京卓越未来国际医药科技发展有限公司企宣部周俊全先生。
张俊华教授从循证评价的需求、循证评价的进展、循证评价的方法三个方面进行了中医药循证评价的关键问题分享。中医药需要循证评价,因为循证医学使临床研究透明化、证据转化规范化、医疗决策科学化。循证医学与中医药学正从碰撞走向融合,这些显著变化表现在从重视病例报告转向重视随机对照试验,从单中心转向多中心研究,从小样本探索转向大样本确证性研究,从重视研究结果到重视研究设计和过程质量控制。基于临床研究中评价指标存在的各种问题,为了更好的推广循证评价方法学的普及和应用,张教授和其团队成立了中医药核心指标集研究中心并建立了ChiCOS研究平台,并发布了团体标准、实践手册、关键技术流程等。
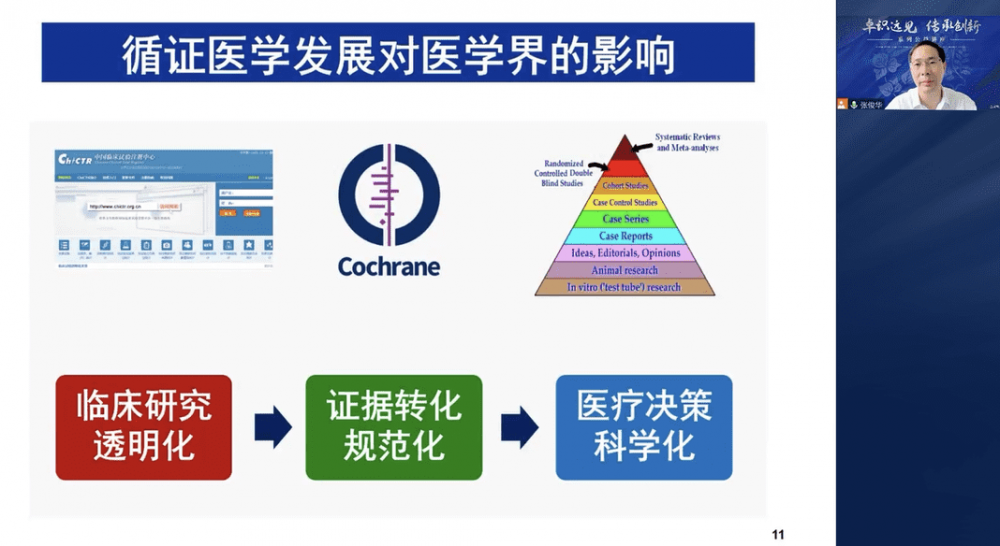
张俊华教授:中医药循证评价的关键问题
周燕文主任作了临床试验的“源”的主题报告。《药品管理法》、《药品注册管理办法》、《药物临床试验质量管理规范》等是药物临床试验的法规要求。周主任详细介绍了GCP中源文件和源数据的定义、包括的内容、源文件的存在形式。临床试验数据管理应遵循ALCOA+CCEA原则,确保试验数据真实、准确、完整、可靠。此外,合格的研究者是数据“源”的保障,规范数据的修改是确保“源”的系统措施。遵循GCP的相关规定,保证药物临床试验过程规范,从源头上保证药品安全、有效,保护受试者权益和安全。
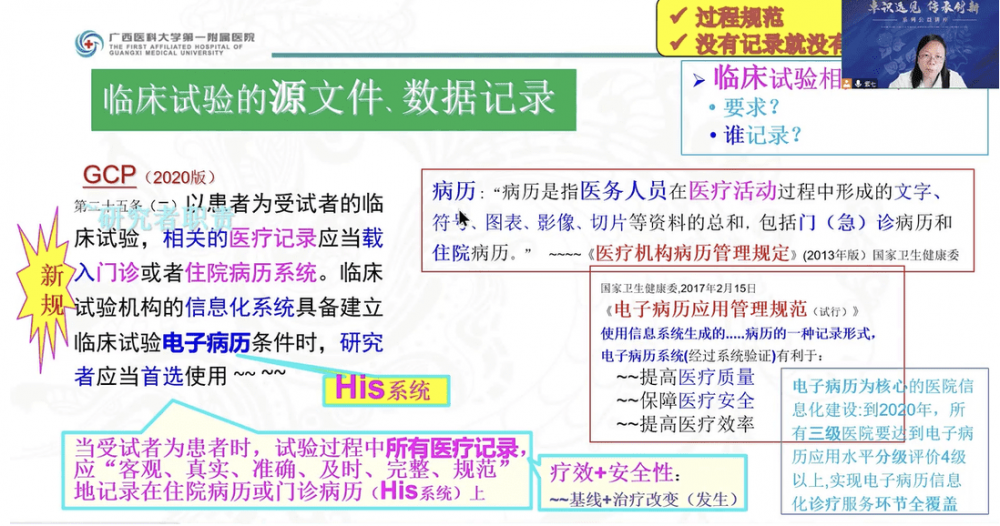
周燕文主任:临床试验的“源”
北京卓越未来国际医药科技发展有限公司是一家专注为药品、医疗器械研发及生产企业、科研机构等提供专业临床试验全产业链技术服务的合同研究组织(CRO),成立于2002年。北京卓越未来国际医药科技发展有限公司将进一步推动我国医药研发、助力临床科研水平的提升。“卓识远见,传承创新”系列公益讲座将于每月10日及20日20:30-22:00在线上滚动播出,期待您的实时关注。